(二)分项情况
1.境内第三类医疗器械注册受理情况
境内第三类医疗器械注册受理共8766项,其中医疗器械注册申请6763项,体外诊断试剂注册申请2003项。
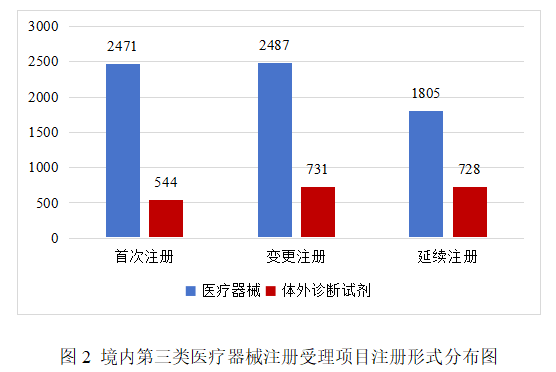
从注册形式看,首次注册3015项,占全部境内第三类医疗器械注册申请数量的34.4%;延续注册2533项,占全部境内第三类医疗器械注册申请数量的28.9%;变更注册3218项,占全部境内第三类医疗器械注册申请数量的36.7%。注册形式分布情况见图2。
2.进口第二类医疗器械注册受理情况
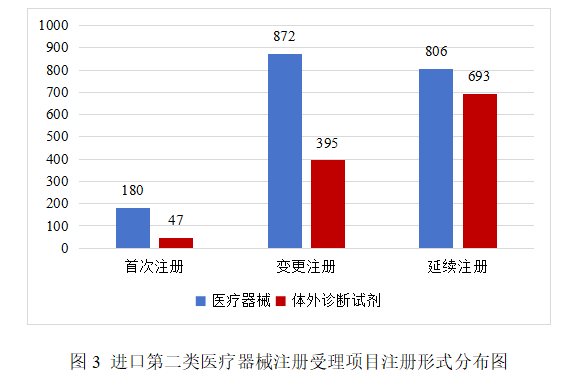
进口第二类医疗器械注册受理共2993项,其中医疗器械注册申请1858项,体外诊断试剂注册申请1135项。
从注册形式看,首次注册227项,占全部进口第二类医疗器械注册申请数量的7.6%;延续注册1499项,占全部进口第二类医疗器械注册申请数量的50.1%;变更注册1267项,占全部进口第二类医疗器械注册申请数量的42.3%。注册形式分布情况见图3。
3.进口第三类医疗器械注册受理情况
进口第三类医疗器械注册受理共2888项,其中医疗器械注册申请2485项,体外诊断试剂注册申请403项。
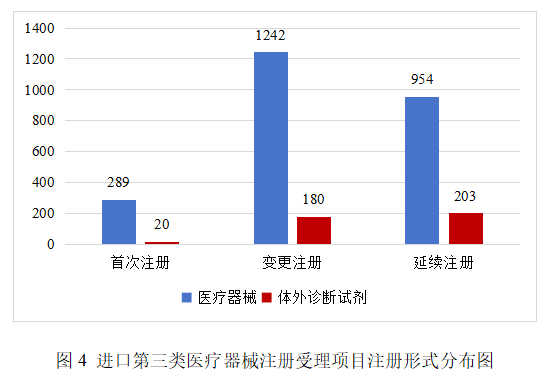
从注册形式看,首次注册309项,占全部进口第三类医疗器械注册申请数量的10.7%;延续注册1157项,占全部进口第三类医疗器械注册申请数量的40.1%;变更注册1422项,占全部进口第三类医疗器械注册申请数量的49.2%。注册形式分布情况见图4。
三、医疗器械注册审批情况
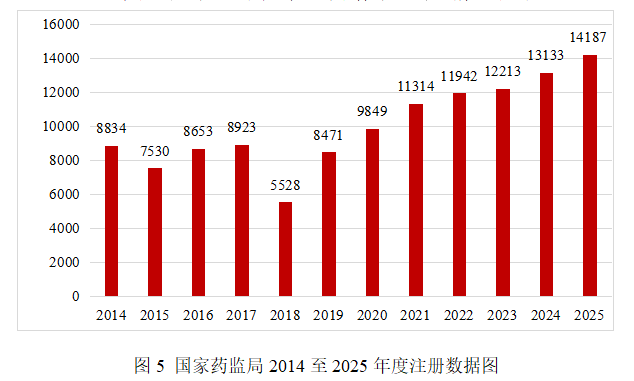
2025年,国家药监局共批准医疗器械首次注册、延续注册和变更注册14187项,与2024年相比注册批准总数量增长8%。
其中,首次注册3402项,延续注册5056项,变更注册5729项。
2025年,企业自行撤回首次注册申请、自行注销注册证书331项。
近12年国家药监局批准医疗器械注册情况见图5。
(一)整体情况
2025年,国家药监局批准境内第三类医疗器械注册8147项,进口医疗器械6040项。
按照注册品种区分,医疗器械10621项,占全部医疗器械注册数量的74.9%;体外诊断试剂3566项,占全部医疗器械注册数量的25.1%。
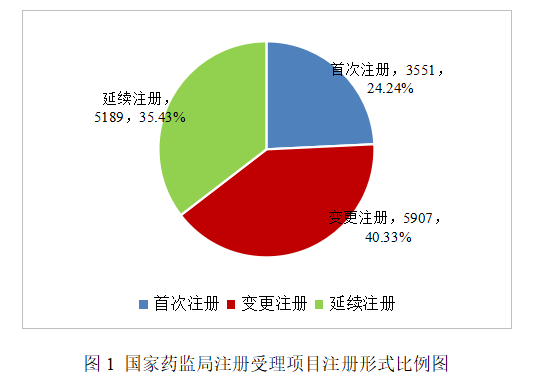
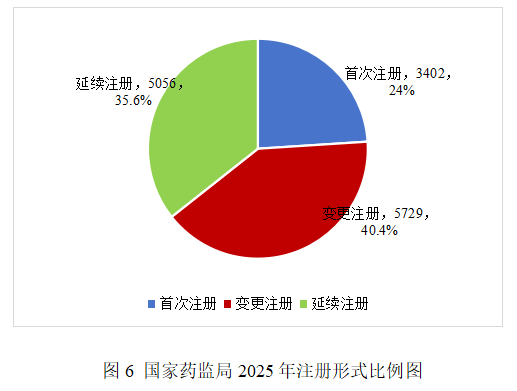
按照注册形式区分,首次注册3402项,占全部医疗器械注册数量的24%;延续注册5056项,占全部医疗器械注册数量的35.6%;变更注册5729项,占全部医疗器械注册数量的40.4%。注册形式比例情况见图6。
(二)分项情况
1.境内第三类医疗器械注册审批情况
境内第三类医疗器械注册8147项。其中,医疗器械6204项,体外诊断试剂1943项。
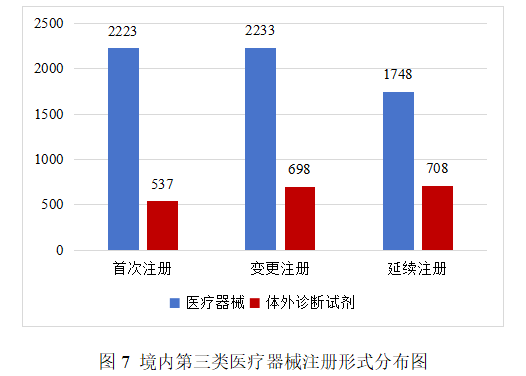
从注册形式看,首次注册2760项,占全部境内第三类医疗器械注册数量的33.9%,延续注册2456项,占全部境内第三类医疗器械注册数量的30.1%;变更注册2931项,占全部境内第三类医疗器械注册数量的36.0%。注册形式分布情况见图7。
2.进口第二类医疗器械注册审批情况
进口第二类医疗器械3102项。其中,医疗器械注册1907项,体外诊断试剂注册1195项。
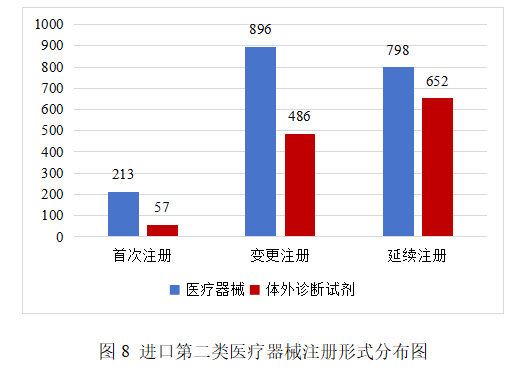
从注册形式看,首次注册270项,占全部进口第二类医疗器械注册数量的8.7%;延续注册1450项,占全部进口第二类医疗器械注册数量的46.7%;变更注册1382项,占全部进口第二类医疗器械注册数量的44.6%。注册形式分布情况见图8。
3.进口第三类医疗器械注册审批情况
进口第三类医疗器械注册2938项。其中,医疗器械注册2510项,体外诊断试剂注册428项。
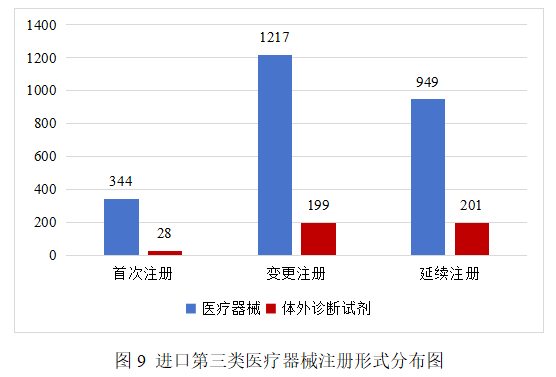
从注册形式看,首次注册372项,占全部进口第三类医疗器械注册数量的12.7%;延续注册1150项,占全部进口第三类医疗器械注册数量的39.1%;变更注册1416项,占全部进口第三类医疗器械注册数量的48.2%。注册形式分布情况见图9。
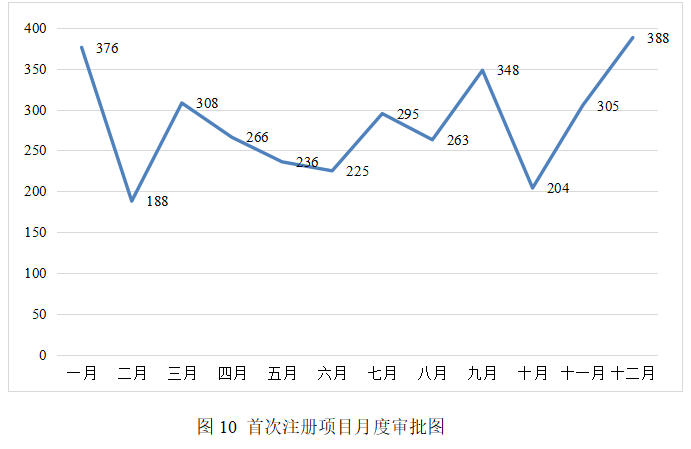
(三)首次注册项目月度审批情况
2025年,国家药监局首次注册月度审批情况见图10。
(四)具体批准品种种类分析
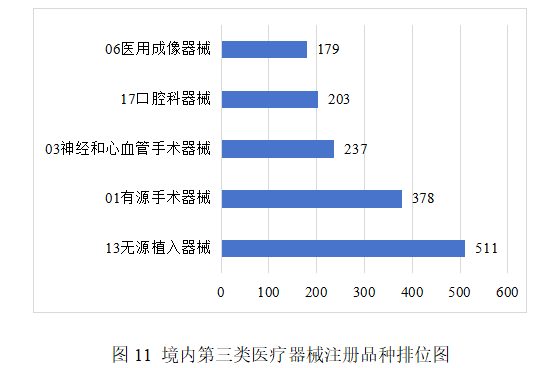
注册的境内第三类医疗器械,除体外诊断试剂外,共涉及《医疗器械分类目录》中18个子目录的产品。
注册数量前五位的境内第三类医疗器械是:无源植入器械,有源手术器械,神经和心血管手术器械,口腔科器械,医用成像器械。与2024年相比,无源植入器械注册数量同比增加5.1%,有源手术器械超过神经和心血管手术器械,注册数量同比增加34.5%,医用成像器械超过注输、护理和防护器械进入前五位,其他品类注册数量有所下降,如注输、护理和防护器械同比减少31.9%,神经和心血管手术器械同比减少19.9%,口腔科器械同比减少1%。
注册的进口医疗器械,除体外诊断试剂外,共涉及《医疗器械分类目录》中21个子目录的产品。
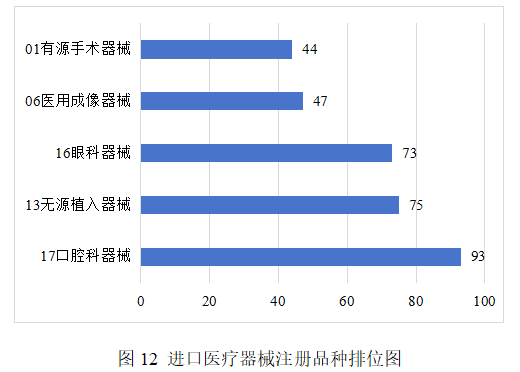
注册数量前五位的进口医疗器械是:口腔科器械,无源植入器械,眼科器械,医用成像器械,有源手术器械。与2024年相比,变化较大,口腔科器械超过无源植入器械,位居第一,注册数量同比增加24%,眼科器械超过有源手术器械,注册数量同比增加35.2%,医用成像器械超过有源植入器械进入前五位,其他品类注册数量略有下降。
(五)进口医疗器械国别情况
2025年,共有30个国家(地区)产品在我国获批上市。
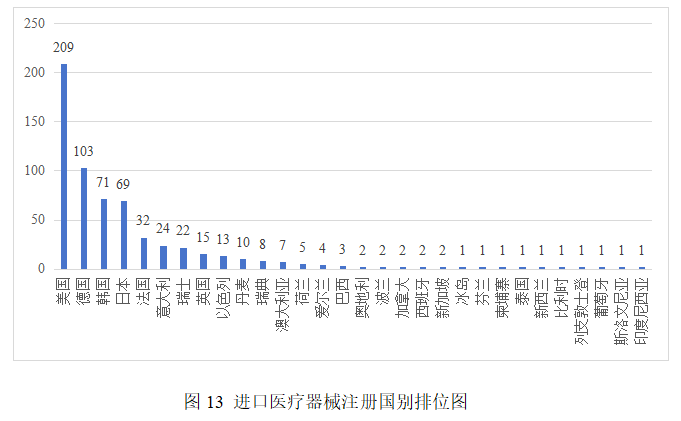
其中,美国、德国、韩国、日本、法国医疗器械在中国医疗器械进口产品首次注册数量位列前5位,注册产品数量约占2025年进口产品首次注册总数量的75.4%。
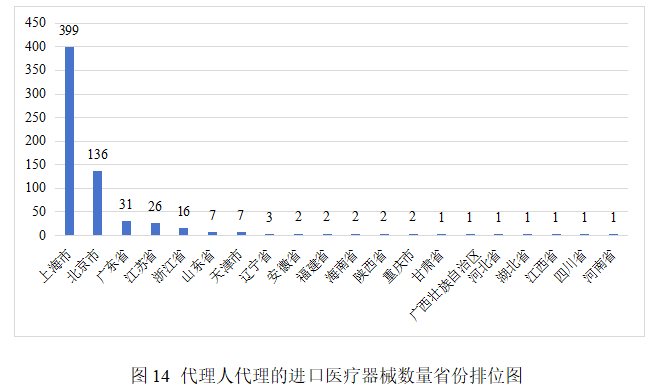
从进口医疗器械代理人分布看,共有19个省涉及有本省企业作为进口医疗器械代理人,其中上海市代理人代理的进口首次医疗器械数量最多,占全部进口医疗器械数量的62.1%。
(六)境内第三类医疗器械省份分析
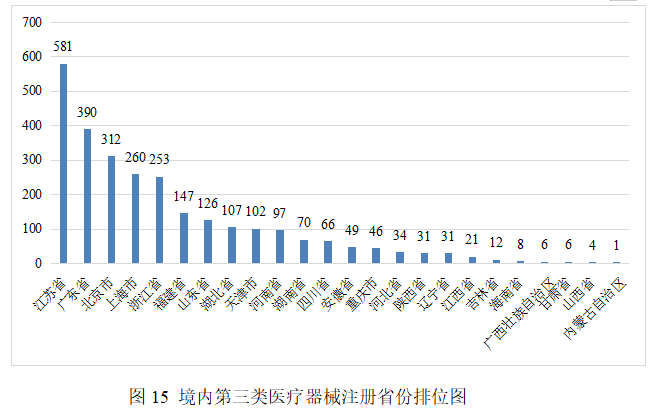
从2025年境内第三类医疗器械注册情况看,相关注册人主要集中在沿海经济较发达省份。
其中,江苏、广东、北京、上海、浙江是境内第三类医疗器械首次注册数量排前五名的省份,占2025年境内第三类医疗器械首次注册数量的65.1%。
四、创新医疗器械等产品注册审批情况
2025年,国家药监局按照《创新医疗器械特别审查程序》《医疗器械优先审批程序》继续做好相关产品的审查工作,共收到创新医疗器械特别审批申请457项,其中104项获准进入创新医疗器械特别审查程序;收到优先申请38项,其中26项获准优先审批。
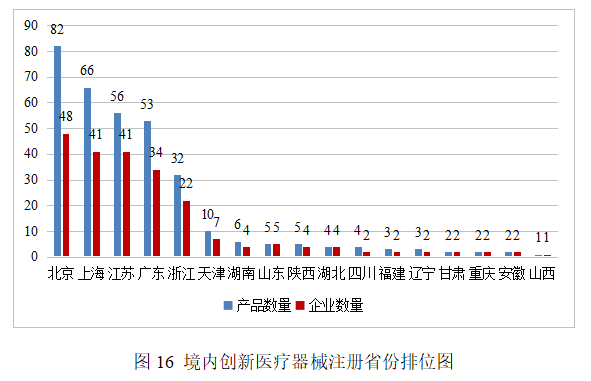
从2014年至2025年,国家药监局共批准391个创新医疗器械。其中境内创新医疗器械336个,涉及17个省的223家企业;进口创新医疗器械55个,涉及6个国家的30个企业。北京、上海、江苏、广东、浙江创新医疗器械获批产品数量和相应企业数量最多,约占全部已批准的391个创新医疗器械的73.9%。
已批准的创新医疗器械中,有源产品占比约61%,无源产品约32%,体外诊断试剂产品约7%,具体见图17。
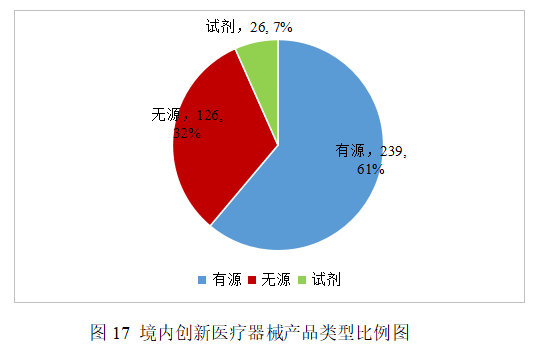
2025年,国家药监局共批准76个创新医疗器械产品上市,相比2024年增加16.9%。其中有源医疗器械45个,无源医疗器械29个,体外诊断试剂2个。
有源手术器械、无源植入器械、有源植入器械、眼科器械、神经和心血管手术器械是2025年批准的创新医疗器械数量前五位的品类,与2024年相比,无源植入器械和眼科器械品类的创新产品增长较快。具体见图18。
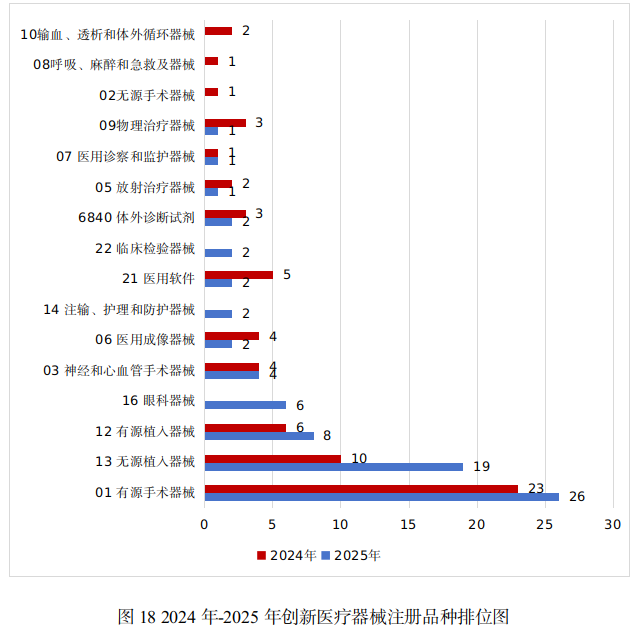
这些创新产品核心技术都有我国的发明专利权或者发明专利申请已经国务院专利行政部门公开,产品主要工作原理/作用机理为国内首创,具有显著的临床应用价值。以下是已批准创新医疗器械产品介绍:
(一)有晶体眼人工晶状体:该产品用于成年人有晶状体眼的治疗,矫正/降低成年人-3.25D-18.00D的近视度数。产品采用零球差大光学区及双凹面型的稳定拱高设计,可提升视觉质量,带来更开阔的周边拱高。




