(五十)焦深延长型人工晶状体:该产品为单件式后房人工晶状体,主体部分及襻采用疏水性丙烯酸酯材料。产品前光学区表面为非球面加衍射环设计,后表面为球面,采用多个衍射级次设计,实现焦深延长。适用于成年人白内障摘除手术后无晶状体眼的视力矫正,通过扩展焦深改善中视力以降低对眼镜的依赖程度。
(五十一)磁共振监测半导体激光治疗设备、一次性使用激光光纤套件和立体定向手术计划软件:磁共振监测半导体激光治疗设备由主机和配件组成。一次性使用激光光纤套件由医用光纤导管组件和冷却水管组成。立体定向手术计划软件由安装U盘、密钥组成。磁共振监测半导体激光治疗设备与一次性使用激光光纤套件配合,用于对药物难治性癫痫患者(局灶性发作,有明确的致痫区部位或明确的癫痫传导途径)的局部病灶进行激光治疗。立体定向手术计划软件与磁共振监测半导体激光治疗设备配合,用于头部立体定向手术计划制定。该产品可最大程度减少手术通路对正常脑组织的损伤,能更好保留认知功能。
(五十二)心脏电生理介入手术控制系统:该产品由执行器(含前端机械臂和前端驱动平台、后端机械臂和后端驱动平台)、操作器、工作站组成。产品与一次性使用电生理介入器械控制系统传输部件配合使用,辅助临床医师用于房颤导管射频消融术期间,操控兼容的压力监测射频消融导管和鞘管。该产品采用遥操作系统执行电生理导管消融手术,替代术者在床旁手动操作导管和鞘管的传统术式,产品在术中可实时图形化导鞘关系,解决传统手术中固定弯鞘管在三维标测系统内不可视的问题,手术安全性更高。
(五十三)前列腺癌磁共振图像辅助检测软件:该产品由软件安装文件组成,功能模块包括:确认模块、设置模块(含基于深度学习的前列腺配置),该产品是采用深度学习技术的人工智能医疗器械,可用于前列腺磁共振图像的显示、处理、测量和分析,对未治疗的40岁及以上成人患者疑似前列腺腺癌病变进行辅助检测,在临床应用中可以提高医生阅片质量,减少不必要的穿刺。
(五十四)胸腹主动脉覆膜支架系统:该产品包括胸腹主动脉主体覆膜支架系统、外周血管覆膜支架系统、主体延长支架系统、分叉型主体支架系统和髂延长支架系统。该产品用于胸腹主动脉瘤的腔内修复。适用的人群需满足以下条件:良好的股、髂和上肢动脉入路;胸腹主动脉瘤近端锚定区直径范围为17-36mm,近端锚定区长度>25mm;内脏分支血管锚定区直径范围为6-13mm,长度≥15mm;肾动脉锚定区直径范围为4.5-9mm;长度≥15mm;远端锚定区:如果远端锚定区在髂动脉,则髂动脉直径范围7-25mm,长度≥15mm;如果远端锚定区在主动脉,则主动脉直径范围12-36mm,长度≥20mm。
(五十五)一次性使用压力监测心脏脉冲电场消融导管:该产品由导管和连接尾线组成,基于应变片原理的压力传感器设计,结合脉冲电场技术、磁场定位技术、盐水灌注技术,与心脏脉冲电场消融设备配合使用,可用于房室结折返性心动过速和房室折返性心动过速的治疗;与三维心脏电生理标测系统配合使用,可提供导管在心内的位置信息以及进行导管头端和心壁之间触点压力的实时测量。该产品为室上性心动过速治疗提供了更多选择。
(五十六)分支型主动脉术中支架系统:该产品由带有分支的支架及输送器组成。其中支架由覆有PTFE膜的镍钛合金支架、不锈钢连接套管、PET管状涤纶布(带标识线)及包膜缝线、人造血管、聚四氟乙烯的缝合线、包膜、包膜固定线组成。人造血管材质为PET、胶原、甘油。输送器由大软管、小软管、释放旋钮等部件组成,其中释放旋钮通过释放拉线分别连接支架的不同位置,可使支架分段释放。该产品适用于Stanford A型主动脉夹层的外科开放手术治疗。
(五十七)经导管主动脉瓣系统:该产品主动脉瓣的定位键设计预期可实现瓣膜精确定位与锚定;流出端大网孔设计预期可降低冠状动脉患者后期冠脉再介入治疗的难度;流入端菱形网孔高密度设计预期可提供良好的封堵效果。输送器的可调弯设计和可旋转设计预期可提高瓣膜定位和释放的精确性。产品适用于经心脏团队评估认为有症状、重度主动脉瓣反流(大于等于3级),不适合进行常规外科手术置换瓣膜、年龄大于等于70岁的患者。
(五十八)一次性使用无菌导尿管:该产品分为单腔、双腔和三腔型。导尿管管身外表面含有聚赖氨酸涂层,基于聚赖氨酸与细菌细胞膜的电荷相互作用机制,以直接接触方式发挥抑菌作用,减少细菌在导尿管表面的定植和生长。
(五十九)质子治疗系统:该产品由加速器子系统和治疗子系统组成,加速器子系统包括主加速器系统、能量选择系统和射束传输系统,治疗子系统包括360°旋转束治疗系统和治疗计划系统,适用于治疗全身实体恶性肿瘤及特定良性疾病。该产品采用悬臂式机架的小型化设计,可节约质子设备的空间、提高治疗效率。
(六十)植入式脑深部神经刺激器、植入式脑深部神经刺激电极导线和植入式脑深部神经刺激延伸导线:植入式脑深部神经刺激器与植入式脑深部神经刺激电极导线、植入式脑深部神经刺激延伸导线联合使用,组成植入式脑深部神经刺激系统,该系统对伏隔核和内囊前肢进行刺激,用于难治性的中重度阿片类药物成瘾患者的防复发辅助治疗。植入式脑深部神经刺激系统填补了物理性干预阿片类药物成瘾治疗的技术空白,为阿片类药物成瘾患者的治疗提供了更多选择。
(六十一)肿瘤电场治疗仪:该产品由主机、分线盒、一次性使用电极片、电源适配器、锂离子电池、充电座组成,产生固定频率的交变电场作用于脑部,适用于22岁及以上经组织病理学或影像学新诊断的幕上胶质母细胞瘤患者,在手术治疗与放射治疗后,与替莫唑胺(TMZ)联合使用。该产品是首个用于该罕见病治疗的国产产品,预期可提高患者治疗的可及性。
(六十二)介入式左心室辅助设备和介入式左心室辅助导管泵套件:介入式左心室辅助设备和介入式左心室辅助导管泵套件联合使用,用于高风险经皮冠状动脉介入治疗(PCI),为患有严重冠状动脉疾病、左心室射血分数降低且血流动力学稳定的成人患者提供左心室辅助。
五、其他注册管理情况
(一)境内第二类医疗器械注册审批情况
2025年,各省级药品监管部门共批准境内第二类医疗器械注册41925项。其中,首次注册14466项,占全部境内第二类医疗器械注册数量的34.5%;延续注册14060项,占全部境内第二类医疗器械注册数量的33.5%;变更注册13399项,占全部境内第二类医疗器械注册数量的32%(见图19)。2025年各省共注销1857个注册证。
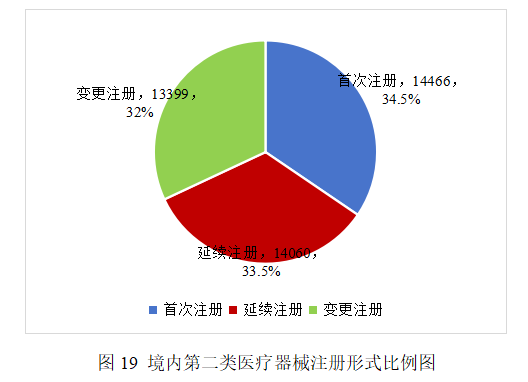
从注册情况看,广东、江苏、北京、河南、浙江、湖南、上海、山东、湖北、河北10省(市)办理境内第二类医疗器械注册事项较多。
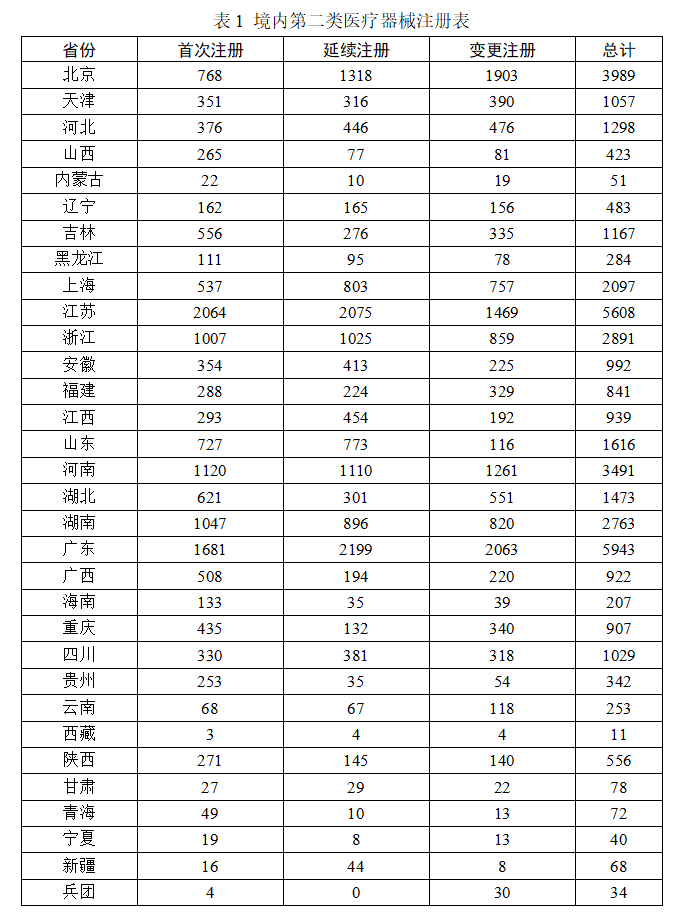
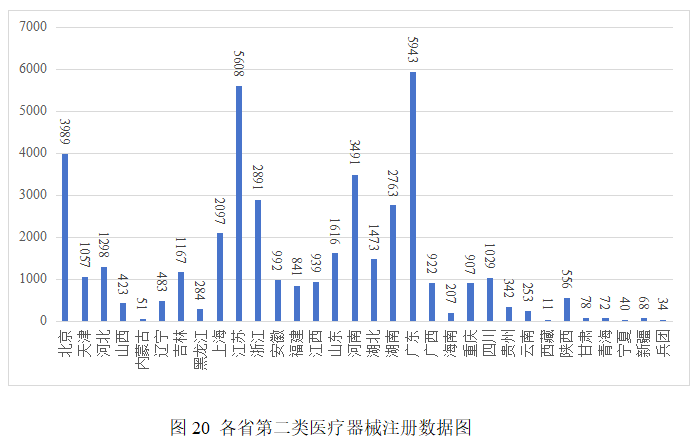
第二类医疗器械注册具体数据见表1及图20。
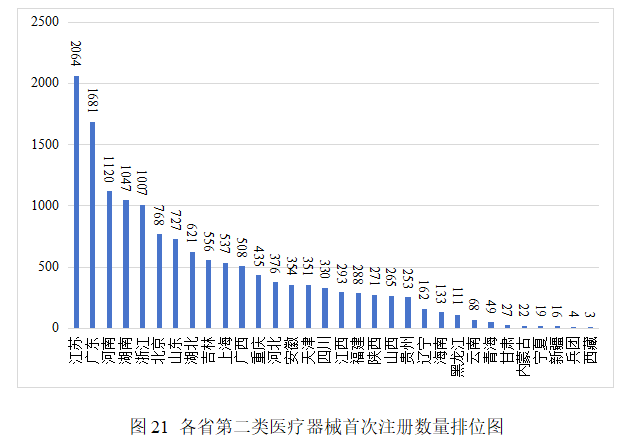
从首次注册情况看,江苏、广东、河南、湖南、浙江、北京、山东、湖北、吉林、上海10省(市)首次注册的境内第二类医疗器械数量较多。各省第二类医疗器械首次注册数量排位图见图21。
(二)第一类医疗器械备案情况
2025年,国家药监局依职责共办理进口第一类医疗器械备案数量1826项。
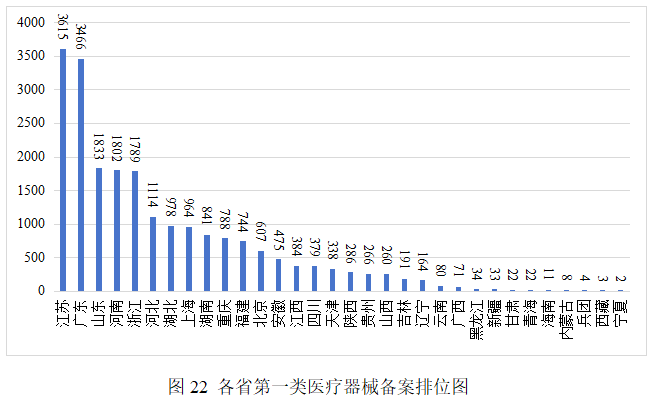
2025年,全国设区的市级药品监管部门依职责共办理境内第一类医疗器械备案数量21574项。其中江苏、广东、山东、河南、浙江是第一类备案数量前五的省份。各省第一类医疗器械备案排位图见图22。
(三)登记事项变更/变更备案情况
2025年,国家药监局依职责共办理进口第二、三类和境内第三类医疗器械变更备案6415项。
其中,境内第三类医疗器械变更备案4546项,进口第二类、三类医疗器械变更备案1869项。




